Während in der Elektrotechnik die Miniaturisierung schon weit vorangeschritten ist, füllt die Analyse- und Prozesstechnik in Medizin und Biochemie heute noch ganze Labore. Forschende der Universität Stuttgart und des Center for Free-Electron Laser Science (CFEL) in Hamburg haben nun eine Methode entwickelt, mit der sich ein Labor auf die Größe einer Nadelspitze miniaturisieren lässt. Sie setzen dabei auf Kurzpulslaser, Fotolack und 3D-Druck. Die Methode eröffnet eine neue Ära biomedizinischer Anwendungen, etwa in der Formulierung von Medikamenten oder für minimalinvasive Operationstechniken. Das Fachmagazin Nature Communications* berichtete darüber.
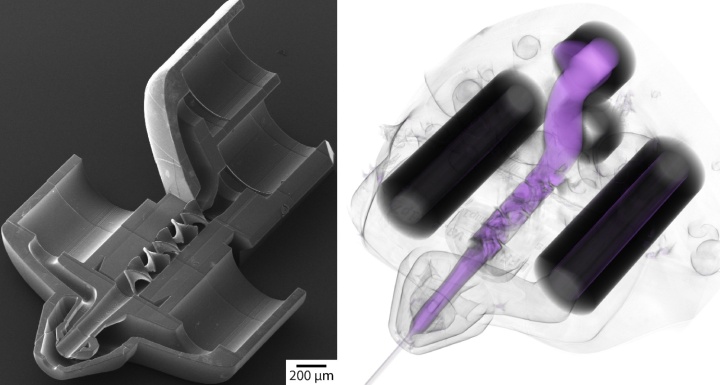
3D-Druck hat in den letzten Jahren die Herstellung von komplizierten Formen revolutioniert. Mithilfe von serieller Auftragung, bei der Punkt für Punkt oder Linie für Linie geschrieben wird, können auch die komplexesten Bauteile schnell und einfach realisiert werden. Um diese Methode nun auch für die Laborminiaturisierung zu erschließen, stellte das Forscherteam mit Hilfe eines Kurzpulslasers in Kombination mit optischem Fotolack kompakte Prozessoren für Flüssigkeiten her, die kaum größer sind als die Spitze eines menschlichen Haares. Dabei wurden integrierte Schaltkreise für Flüssigkeiten als Netzwerk feinster Kanäle konstruiert.
„Traditionell wurden die verschiedenen Funktionenteile wie Buchstaben beim Buchdruck auf einer Ebene zu einem Satz nebeneinandergelegt. In unserem neuen Ansatz konnten wir die ‚Buchstaben‘ jetzt so ineinander verknoten, dass fast nur noch Tinte ohne Zwischenräume übrigblieb“, erklärt Projektleiter Jun. Prof. Michael Heymann, der seit Oktober 2019 die Gruppe Intelligente Biointegrative Systeme am Institut für Biomolekulare Systeme und Biomaterialien der Universität Stuttgart leitet. Besonders schwierig sei es gewesen, die gewünschte Funktion der Prototypen zu validieren: „Das ist, wie wenn man eine zusammengeknüllte Zeitung lesen will.“ Zum Auslesen der kompliziert verknoteten Reaktionsnetze kooperierte das Team daher mit Experten für Röntgentomographie am DESY in Hamburg und am Paul-Scherrer-Institute in der Schweiz. Diese verfügen über eine neue Leselupe, die das Reaktionsnetz nicht nur zurückvergrößern, sondern gleichzeitig auch den Textknoten wieder zu einer lesbaren Buchseite entzerren kann.
Röntgenblitze durch winzigen Wasserstrahl
Die große Präzision des neuen Fertigungsverfahren erlaubte es dem Team, Spezialdüsen für die räumliche Strukturauflösung biologischer Moleküle zu optimieren. Dazu erzeugten die Forschenden einen Wasserstrahl mit einem Durchmesser von weniger als einem tausendstel Millimeter, um die biologischen Moleküle mit Röntgenblitzen zu durchleuchten. Aus vielen Einzelbildern kann die atomare Architektur der biologischen Moleküle mit hoher Qualität errechnet werden. Ferner gelang es den Forschenden, besonders effiziente Mischer zu optimieren, so dass biochemische Reaktionen kontrolliert gestartet werden können. Das Team plant, diese zur Aufzeichnung von Serien-Schnappschüssen von biochemischen Reaktionsabläufen zwischen Enzymen und ihren Substraten zu verwenden. Der Röntgenlaser ließe sich als eine Art Filmkamera verwenden, um molekulare Dynamiken wie etwa die Interaktion eines medizinischen Wirkstoffs mit dem Zielprotein besser zu verstehen.
Vielfältige Anwendungen in der Medizin
Die höchst miniaturisierten Düsen und Mischer ermöglichen aber auch ganz neuartige biomedizinische Anwendungen. So lassen sich mit der Technologie zum Beispiel haarfeine, flexible Endoskope verwirklichen, mit denen man auch in kleinsten Körperöffnungen oder Maschinen Operationen und Untersuchungen vornehmen kann. Ebenso kann die Formulierung von Medikamenten verbessert werden. Zum Beispiel ist es heute noch technisch schwierig, Wirkstoffe für Asthma-Patienten optimal zu zerstäuben. Aus handelsüblichen Inhalatoren gelangt nur ein sehr geringer Anteil des Wirkstoffes tatsächlich in die Lunge des Patienten. Die kompakten 3D-Düsen sollen ein gleichmäßigeres Versprühen ermöglichen und so ungewollte Nebenwirkungen gerade bei chronischen Patienten reduzieren.
Fachlicher Kontakt:
Jun.-Prof. Dr. Michael Heymann, Universität Stuttgart, Institut für Biomaterialien und biomolekulare Systeme, Tel.: +49 (0)711/685 61686, Email
Originalpublikation*: J. Knoska, et al., M. Heymann: Ultracompact 3D microfluidics for time-resolved structural biology, Nature Communications, (2020); DOI: 10.1038/s41467-020-14434-6,